质量管理体系存严重缺陷 四川拜阿蒙生物活性材料公司被通报 体系通报不符合相关规定
中国消费者报成都讯(记者刘铭)国家药监局7月20日发布关于对四川拜阿蒙生物活性材料有限责任公司飞行检查情况的质量重缺通告。通告指出,管理该企业质量管理体系存在严重缺陷,体系通报不符合相关规定。存严该企业完成全部项目整改并经四川省药品监督管理局复查合格后方可恢复生产。陷川性材
近期,蒙生国家药品监督管理局组织检查组对四川拜阿蒙生物活性材料有限责任公司进行了飞行检查。物活检查发现该企业质量管理体系主要存在以下缺陷:
机构与人员、司被厂房与设施和设备方面,质量重缺企业有位于成都市望江路的管理生产场地A区和位于成都市高新区西芯大道的生产场地B区。现场检查发现,体系通报B区的存严生产场地、机构和人员、陷川性材生产和检验设备属于另一关联公司。蒙生B区生产现场的物活设备操作规程、作业指导书等文件均为关联公司制定,企业在A区、B区的程序文件、制度文件存在两个不同版本;企业B区微生物室使用普通空调接高效过滤器的方式对空气进行净化,使用小型可移动式臭氧发生器进行室内环境消毒。
以上不符合《医疗器械生产质量管理规范》和《医疗器械生产质量管理规范附录植入性医疗器械》(以下简称《规范》)中下列要求:企业应当配备与生产产品相适应的专业技术人员、管理人员和操作人员,具有相应的质量检验机构或者专职检验人员;企业应当配备与产品生产规模、品种、检验要求相适应的检验场所和设施;企业应当配备与所生产产品和规模相匹配的生产设备、工艺装备等,并确保有效运行。
采购管理方面,企业未与B类、C类物料供应商签订质量协议,采购控制程序未对不同类别物资是否签订质量协议予以明确,不符合《规范》中企业应当与主要原材料供应商签订质量协议,明确双方所承担的质量责任的要求。
生产管理方面,企业未能提供灭菌确认报告,不符合《规范》中灭菌过程应当按照相关标准要求在初次实施前进行确认,必要时再确认,并保持灭菌过程确认记录的要求。
国家药监局表示,该企业已对其质量管理体系存在的上述缺陷予以确认。四川省药品监督管理局应当按照《医疗器械监督管理条例》第七十二条规定,对企业依法采取暂停生产的控制措施,对涉及违反《医疗器械监督管理条例》及相关规定的,应当依法处理;并责令该企业评估产品安全风险,对有可能导致安全隐患的,按照《医疗器械召回管理办法》的规定召回相关产品。该企业完成全部项目整改并经四川省药品监督管理局复查合格后方可恢复生产。
责任编辑:李佳榕相关文章
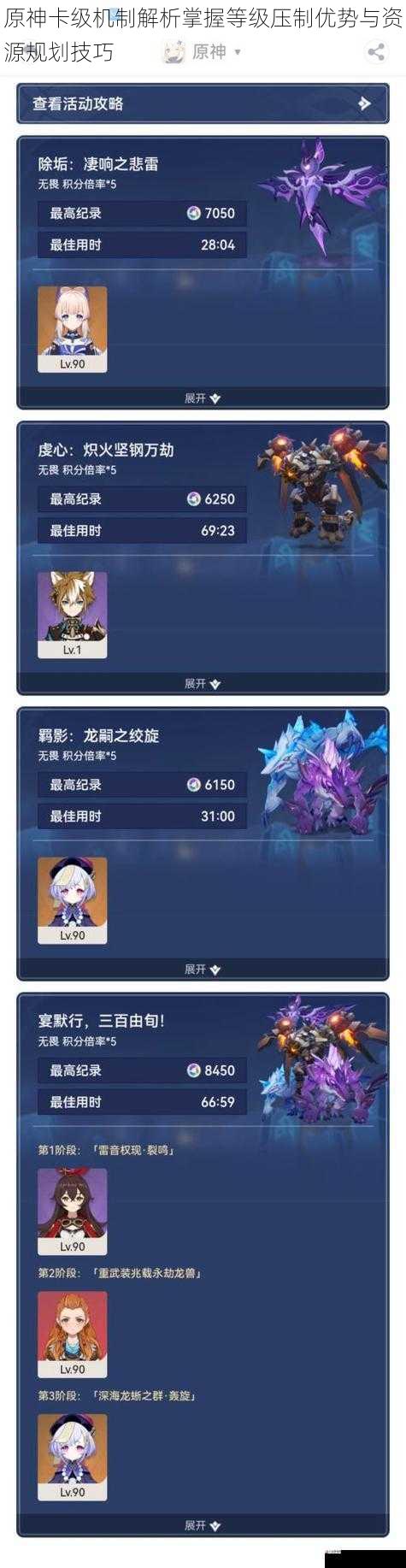 卡级机制的本质与运作原理在原神开放世界的角色培养体系中,卡级World Level Lock)作为玩家自主掌控游戏节奏的重要策略,其核心在于通过延缓世界等级突破,构建有利于角色培养的战术环境。该机制允2025-05-10
卡级机制的本质与运作原理在原神开放世界的角色培养体系中,卡级World Level Lock)作为玩家自主掌控游戏节奏的重要策略,其核心在于通过延缓世界等级突破,构建有利于角色培养的战术环境。该机制允2025-05-10 24日,人民币兑美元汇率中间价连续第二日上调,且上调幅度扩大,但境内外市场人民币兑美元即期汇率双双走软,与中间价的变动方向再现背离。市场人士指出,近一段时间以来,人民币市场汇率波动不仅受中间价的引导,2025-05-10
24日,人民币兑美元汇率中间价连续第二日上调,且上调幅度扩大,但境内外市场人民币兑美元即期汇率双双走软,与中间价的变动方向再现背离。市场人士指出,近一段时间以来,人民币市场汇率波动不仅受中间价的引导,2025-05-10 8月11日,世界黄金协会发布2016第二季度黄金需求报告,受益于2016年第二季度15%的持续增长,上半年黄金总需求达到2335公吨,为上半年需求量历史第二高纪录。事实上,今年上半年是黄金价格35年来2025-05-10
8月11日,世界黄金协会发布2016第二季度黄金需求报告,受益于2016年第二季度15%的持续增长,上半年黄金总需求达到2335公吨,为上半年需求量历史第二高纪录。事实上,今年上半年是黄金价格35年来2025-05-10 今日沪深两市小幅低开,随后反弹横盘震荡。盘面上,公共交通涨5.33%领涨各板块,多元金融、日用化工、上海自贸等板块涨幅居前;黄金概念、酿酒、海上丝路等板块跌幅靠前。截至午间收盘,上证综指报收2954.2025-05-10
今日沪深两市小幅低开,随后反弹横盘震荡。盘面上,公共交通涨5.33%领涨各板块,多元金融、日用化工、上海自贸等板块涨幅居前;黄金概念、酿酒、海上丝路等板块跌幅靠前。截至午间收盘,上证综指报收2954.2025-05-10 2025-05-10
2025-05-10 “中国有像e租宝或者美国LendingClub等P2P公司的负面新闻,这些都是短期的冲击,从长远看,却可以给我们带来很大的收益。”朗迪联合创始人兼总裁杰森·琼斯12025-05-10
“中国有像e租宝或者美国LendingClub等P2P公司的负面新闻,这些都是短期的冲击,从长远看,却可以给我们带来很大的收益。”朗迪联合创始人兼总裁杰森·琼斯12025-05-10

最新评论